获得突破性疗法认定,对一个新药的意义有多大?
本文来自微信公众号“医药魔方”,作者 April Chen。
百济神州(06160)的BTK抑制剂BGB-3111 (zanubrutinib)是2019年首个获得FDA突破性疗法认定的肿瘤药,获得这一认定到底有什么意义呢?我们先来了解一下FDA的一些特殊审批通道。
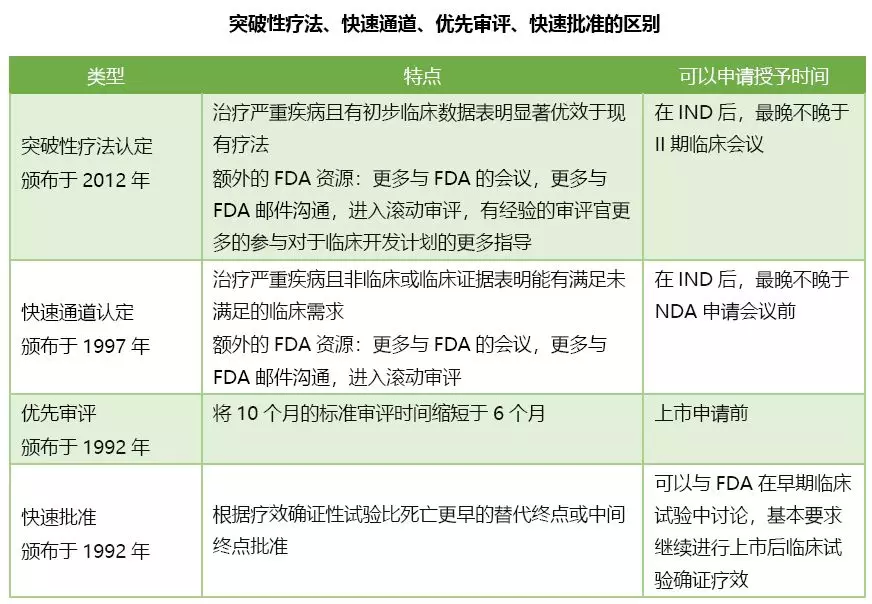
突破性疗法(BTD)的资格认定可以在较早临床开发阶段授予给某个药物, 让其得到FDA更多的支持,包括FDA给申办方提出的关于中期分析,研究之间数据桥接的方法,研究规模缩减和定制设计的终点的建议,FDA的反馈时间也会缩短到不超过60天。
那么,获得突破性疗法认定是否能缩短新药获批上市的时间呢?2013年11月,罗氏/Genentech的Gazyva(obinutuzumab) 和强生/ Pharmacyclics的Imbruvica (ibrutinib) 成为最早以突破性疗法认定途径获得FDA批准的两个肿瘤药,但是这两个药物的研发历程并不相同。
Gazyva (奥妥珠单抗)是罗氏开发的第二代CD20人源化单抗,与利妥昔单抗作用机制类似。在2013年4月完成III期临床试验后递交上市申请,2013年5月获得突破性疗法资格认定,同年7月获得FDA优先审评,且在同年11月1日获批与苯丁酸氮芥联用一线治疗CLL。因为奥妥珠单抗获得认定时候已是临床开发晚期,所以其从临床I期到上市共花费约6年,在时间上并没有缩短。
相对来说, Imbruvica(伊布替尼)的研发历程要快的多。在临床II期试验结束后的2013年2和4月分别获得单药治疗套细胞淋巴瘤(MCL)和单药治疗染色体17p缺失的CLL/SLL的BTD。同年6月强生递交两个适应症的上市申请,但2013年11月13日,FDA决定先批准单药用于MCL二线治疗。从I期临床到上市大约花费了4.75年的时间。
以BTD身份被FDA首次批准上市肿瘤药的研发历程(年)
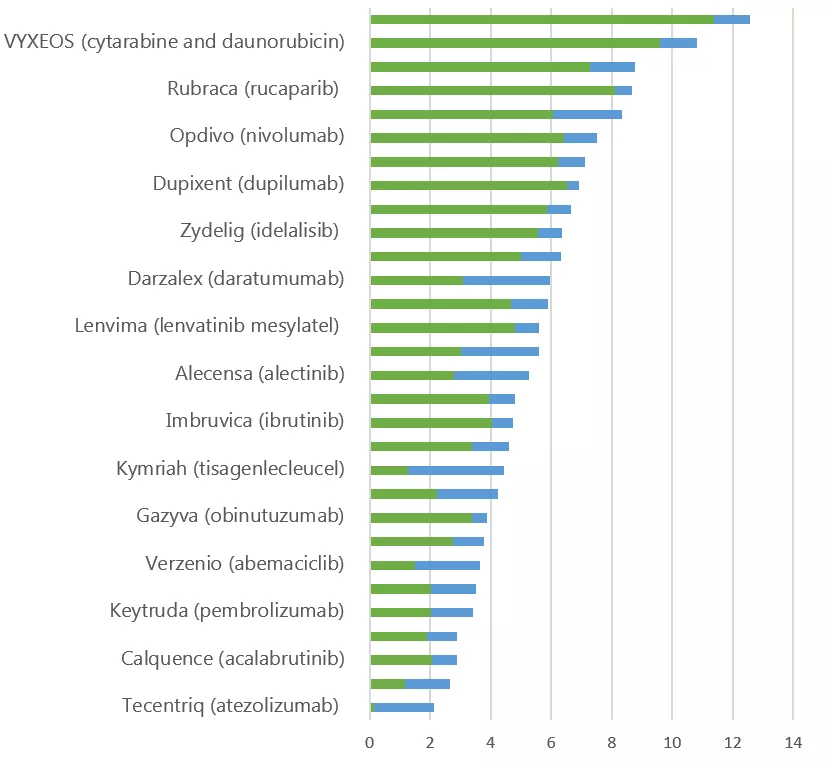
绿色:从临床试验开始到获得BTD的时间;蓝色:从获得BTD到获批上市的时间
从上图可以发现,以BTD身份首次获得FDA批准上市的肿瘤药的临床开发时间约为5.67± 2.44年,相比大多数药物从临床到获批需要大约10年而言还是大大缩短了。如果药物能在临床开发的更早期获得BTD,批准上市的时间会更短。
有一点不可忽视的是,鉴于这些药物的临床价值其,他们并不一定需要获得BTD认定才能赢得FDA的批准,但是正因为在临床早期就展示了足够的突破性,大大加快了上市的进程。
BTD资格认定不是获批上市的承诺
与其他批准路径不同,BTD更强调某种药物相比现有疗法的突破性。公众的反应很可能被放大到这个疗法具有“奇迹”或“治愈”的效应,特别是通过BTD认定上市的药物中绝大多数为肿瘤药。但实际上某个疗法只需满足一定的标准就可以获得BTD资格认定,而不是要求治愈某个疾病。
2013-2018年FDA批准上市的突破性药物数量(按适应症计)
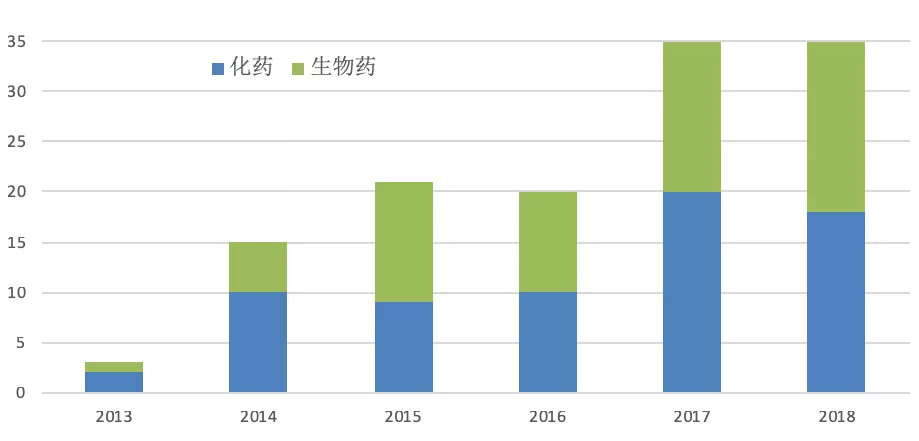
对于生物医药股的投资者来说,一个重要的信息就是了解哪一个药物会有相对较高的概率获得FDA批准,拿到BTD认定显然会提高获批的概率。
FDA批准的突破性药物的疾病领域分布(按适应症计)
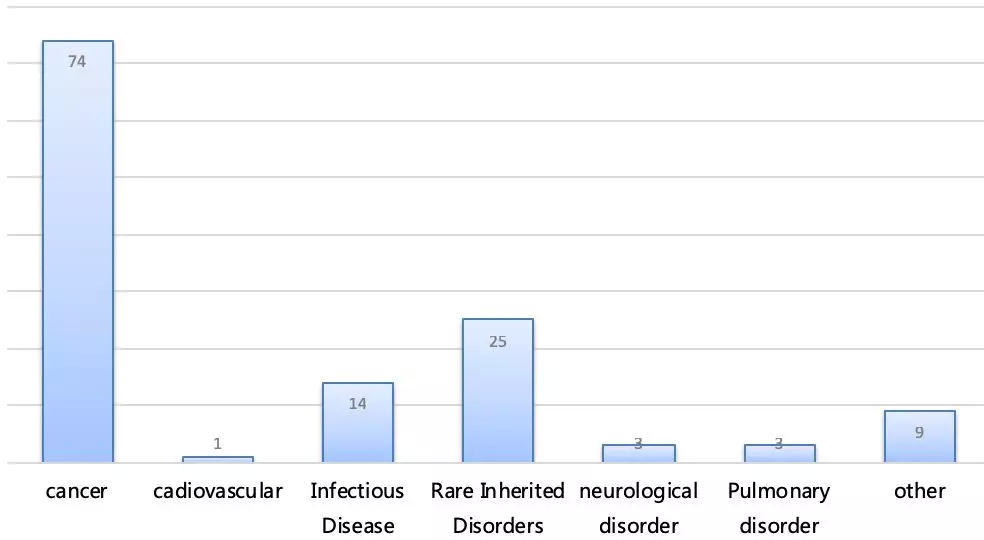
但是一定要注意的是,获得BTD资格认定可以加速一个新药的上市历程,但并不代表一定能够被FDA批准上市,而且BTD资格在授出后也可能会被FDA撤销。
FDA撤销BTD资格的药物
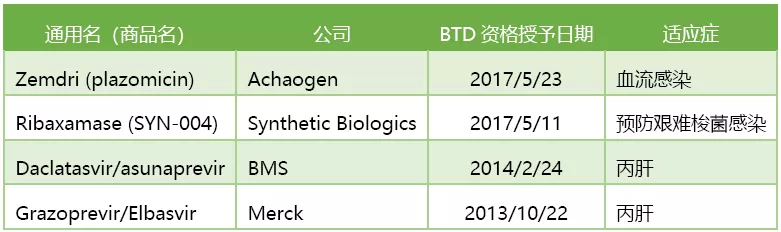
2015年,FDA首次撤回了两个丙肝药物的突破性疗法认定,来自默沙东的Grazoprevir/Elbasvir和BMS的Daclatasvir/asunaprevir复方,因为丙肝领域的新药研发进展过于迅速,FDA在2014年10月批准了Gilead的复方药Harvoni (ledipasvir/sofosbuvir)之后,又重新审视之前授出的突破性疗法。
Ribaxamase (SYN-004)是一个口服β内酰胺酶抗生素,在SYN-004 IIb试验中相比安慰剂可使艰难梭菌感染风险降低71.4%,以此获得FDA的BTD资格。但是在III期试验中,Synthetic Biologics公司称出于安全考虑,自己申请撤回BTD。FDA也表示由于安全数据不完整,无法对试验中观察到的致命性不良事件进行全面评估。
Zemdri (plazomicin) 是新一代氨基糖苷类抗生素,对多种革兰氏阴性菌有效,在2016年批准用于复杂尿路感染,包括肾盂肾炎,2017年5月获得血流感染这一适应症的突破性疗法认定,但在名为ACHN-490-007的III期试验中,由于样本量远少于预期,仅入组37人而不是预期的286人,使得统计上难以证明比对照组粘菌素优效,于2018年6月27日被撤销Zemdri(plazomicin)针对这一适应症的突破性疗法认定,并且上市遥遥无期。
虽然获得FDA的BTD认定不是百分百的上市保障,但对制药企业研发工作的激励作用很明显,并且能够帮助企业获得的资本市场的青睐和助力。BTD认定对小型生物制药企业的影响也更加明显。例如Exelixis的cabozantinib在2012年被FDA首次批准,用于治疗不可手术切除的恶性局部晚期或转移性甲状腺髓样癌(MTC)。由于是罕见类型的甲状腺癌,销量一直没有起色。2015年4月,cabozantinib凭借III期METEOR中二线治疗晚期肾细胞癌相比everolimus组可降低疾病进展风险42%而获得BTD认定。在获得认定之初,Exelixis的股价是7美元,18个月后的今天股价大约在21美元。 在此过程中,Exelixis减少了债务,扩大管线,并与武田就cabozantinib在日本地区的开发权益达成合作。




 扫码下载智通APP
扫码下载智通APP