特朗普以身试药,再生元(REGN.US)中和抗体前景如何
本文来自微信公众号“新康界”。
美国卫生事件再起波澜
当中国人民正在欢度中秋国庆双节假期,享受来之不易的抗疫胜利果实时,美国卫生事件波澜再起。10月1日晚(当地时间),美国总统特朗普及其夫人确诊感染病毒。适逢美国总统换届大选,一时舆论哗然。特朗普作为74岁高龄肥胖感染者,增加了人们对其健康状况的担忧。在对因疗法仍处于研发中的背景下,美国总统将接受怎么样的治疗,更加引发外界关注。
10月2日下午(当地时间),白宫发布声明,称特朗普静脉注射了8克再生元制药(REGN.US)的“抗体鸡尾酒”。先前的试验表明在降低病毒载量方面,高剂量似乎比低剂量效果更好,目前临床研发正在进行中。特朗普在接受试验性疗法之后,被转移到沃尔特·里德(Walter Reed)国家军事医学中心——美国总统的“定点医院”。这一消息加剧了外界对特朗普病情的担忧。
10月2日深夜(当地时间),经特朗普同意,白宫医生西恩·康利(Sean Conley)发布消息,称转移总统至沃尔特·里德以便进一步监控,是经过与沃尔特·里德和约翰霍普金斯大学(John Hopkins University)专家咨询的推荐结果。当晚总统表现良好,不需补充氧气,但是在与专科医生协商后,已启动瑞德西韦(remdesivir)治疗。
图表1. 白宫医生西恩·康利发布的消息

来源:Twitter、中康产业资本研究中心
再生元的“抗体鸡尾酒”
对于“人民的希望”瑞德西韦大家并不陌生,它是全球首款获得药监机构批准的创新疗法。今年5月1日,美国FDA授予瑞德西韦紧急使用授权,允许医疗机构在治疗肺炎重症患者时应用。重症标准是患者血氧水平低,需要吸氧治疗或呼吸机等设备支持。那么,特朗普所接受治疗中的“抗体鸡尾酒”(antibody cocktail)又是什么呢?
再生元的REGN-COV2是由两种单抗REGN10933和REGN10987组成的一种“鸡尾酒”疗法。2种单抗分别针对病毒棘突蛋白受体结合域(RBD)的2个独立非重叠的位点,阻断病毒与人体细胞表面的血管紧张素转化酶(ACE)受体结合,从而使其无法进入细胞(图表2)。随后,病毒/抗体复合物被免疫系统清除。两种抗体组合使用可以降低病毒通过基因突变,逃避单抗体治疗的可能性。
图表2. 再生元“抗体鸡尾酒”作用机制示意
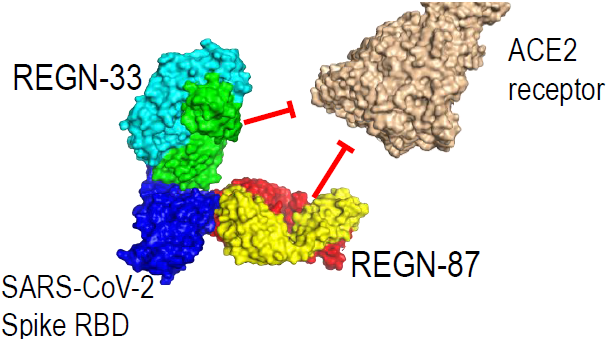
来源:Regeneron公告、中康产业资本研究中心
从作用机制来看,REGN-COV2属于中和抗体疗法,通过与病毒结合阻止其感染人体细胞,发挥“中和作用”。相比疫苗和抗病毒药物,中和抗体疗法具有预防和治疗的双重作用。在非人灵长类动物中的数据显示,在暴露于病毒之前给药,REGN-COV2能够阻断感染;在感染病毒之后给药,REGN-COV2能够导致更快的病毒清除。
中和抗体疗法是直接使用外源性的中和抗体进行被动免疫治疗,相当于为人体免疫系统补充弹药。抗体与病毒结合被消耗后,需要补充外源性的抗体。因此,中和抗体疗法只能用于短期预防和治疗,需要间隔一段时间再次给药。如果要实现大规模的全民免疫,还是需要研发预防性疫苗。疫苗研发周期较长,即使在卫生事件期间平行进行多个步骤,仍然需要1-5年的时间。中和抗体疗法的研发周期则可以相对较短,如果一切顺利,8-12个月就有望研发成功。在疫苗上市之前,中和抗体疗法可以为特定高危人群提供预防;在疫苗上市前后,中和抗体疗法均可用于治疗病毒感染者。
中和抗体药物作为一类颇具潜力的防治疗法,吸引了全球众多制药企业和研发机构开展研发。据Antibody Therapeutics数据库统计,截至2020年9月,全球共有98个靶向病毒棘突蛋白的中和抗体项目。中和抗体药物研发最重要的速度,在卫生事件结束和预防性疫苗上市并大量供应之前上市,才具有价值。中和抗体药物面临“短期存在的蓝海市场”,只有抢先上市才能获得竞争优势。目前研发进度较快的是REGN-COV2,已进入临床III期试验,LY-CoV555(LY3819253)紧随其后。(图表3)
图表3. 病毒中和抗体的临床试验(部分)
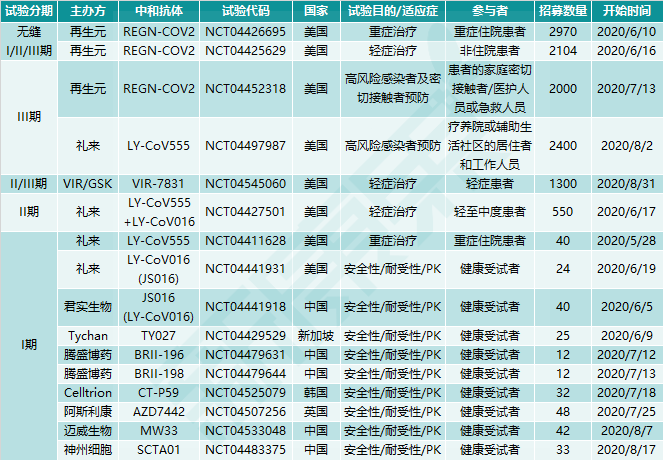
来源:clinicaltrials.org、公司官网、中康产业资本研究中心
全球范围内的中和抗体项目,研发进展较快的有再生元的REGN-COV2,以及礼来与加拿大AbCellera公司联合开发的LY-CoV555,均已进入临床III期。Vir Biotechnology联合GSK开发的单抗VIR-7831已于8月底进入临床II/III期试验,另一款单抗VIR-7831预计在2020年开展临床试验。
国内中和抗体项目已经进入临床阶段的包括:君实生物和中科院微生物所联合开发的JS016、腾盛博药的BRII-196和BRII-198、迈威生物的MW33和神州细胞的SCTA01。君实生物的JS016是中国第一、全球第二进入临床试验的病毒中和抗体疗法。礼来与君实生物在今年5月达成协议,以最高2.55亿美元买断大中华区以外的临床开发和商业化权益。
REGN-COV2现有试验数据
9月29日(美国时间),再生元公布了REGN-COV2治疗轻症非住院成年患者无缝I/II/III期试验(NCT04425629)的最新阶段性结果。公布的数据来自试验招募的首批275名患者,旨在评估抗体鸡尾酒的抗病毒活性,并确定最有可能从治疗中获益的患者。受试者按1:1:1随机分为3组,一次性静脉注射8g(高剂量,REGN10933和REGN10987各4g)、2.4g(低剂量,两种单抗各1.2g)或安慰剂(图表4)。
图表4. 数据切片(首批275例患者)的试验设计
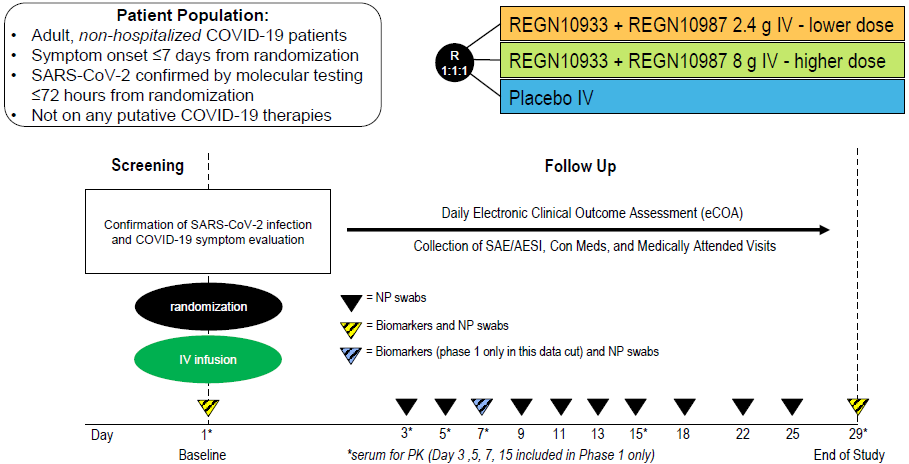
来源:Regeneron公告、中康产业资本研究中心
患者在开始试验前通过血清学测试确定是否已经自行产生抗病毒抗体。大约45%的患者为血清阳性(可检测到抗病毒抗体),41%的患者为血清阴性(不能检测到抗病毒抗体),另外14%的患者血清学状况未知。试验数据分析发现血清学状态与基线病毒载量高度相关(p<0.0001)。血清阳性患者(123例)的平均基线病毒水平低的多(3.49log10拷贝/毫升),即使不进行治疗,病毒载量也迅速接近最低可量化水平(LLQ)。相比而言,血清阴性患者(113例)的平均基线病毒水平(7.18log10拷贝/毫升)明显更高,在不进行治疗的情况下病毒清除的速度更慢。REGN-COV2迅速降低血清阴性患者的病毒载量,在第7天(Day 7)时达到关键病毒学终点。观察血清阴性组的鼻咽(NP)病毒载量从基线到第7天的时间加权平均变化的均值,与安慰剂相比,高剂量治疗组患者减少0.60log10拷贝/毫升(p=0.03),低剂量治疗组患者减少0.51log10拷贝/毫升(p=0.06),REGN-COV2治疗组患者减少0.56log10拷贝/毫升(p=0.02)。基线病毒水平越高的患者,在REGN-COV2治疗第7天时的病毒载量相应减少的越多。
图表5. 血清阴性患者病毒载量的时间加权平均变化
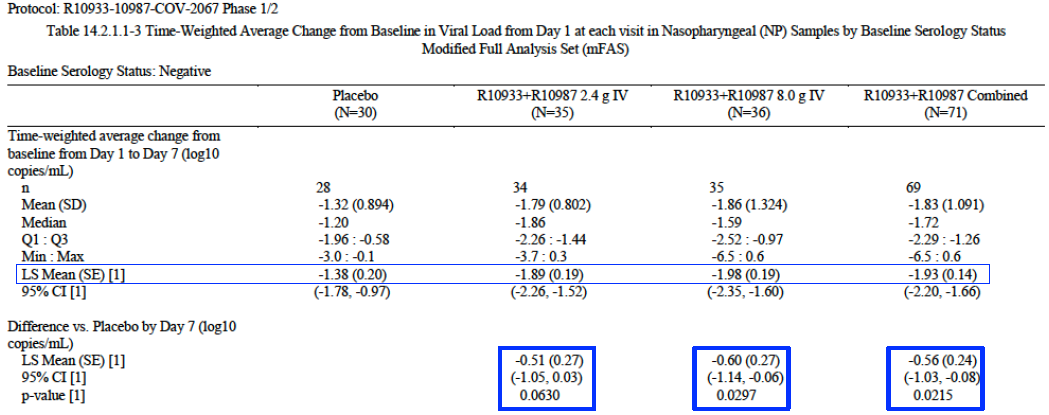
来源:Regeneron公告、中康产业资本研究中心
血清阴性患者和/或基线病毒水平较高的患者在症状缓解方面有更大的获益。对于血清阴性患者的症状缓解(定义为症状变得轻微或消失)平均时间,安慰剂组是13天,高剂量组是8天(p=0.22),低剂量组是6天(p=0.09)。随着基线病毒载量的增加,患者在症状缓解方面的获益也相应增加。
在安全性方面,REGN-COV2的两种剂量(8.0g和2.4g)都耐受良好。4例患者出现输液反应,其中2例使用安慰剂,另外2例使用REGN-COV2。4例患者出现严重不良事件,其中2例使用安慰剂,1例使用低剂量REGN-COV2,还有1例使用高剂量REGN-COV2。试验无死亡病例。已有超过2000人被招募参与REGN-COV2的整个开发项目,独立数据监测委员会没有报告以外的安全性发现。
结语
鉴于再生元目前仅公布了首批275例患者的数据,要想提交上市申请尚需更多的数据。此时,美国总统特朗普作为名人政要,其对于再生元中和抗体疗法的反映,不论是真实还是有所偏差,都必定会对REGN-COV2的审批产生重大影响。后续结果如何,让我们拭目以待。
(编辑:玉景)



 扫码下载智通APP
扫码下载智通APP